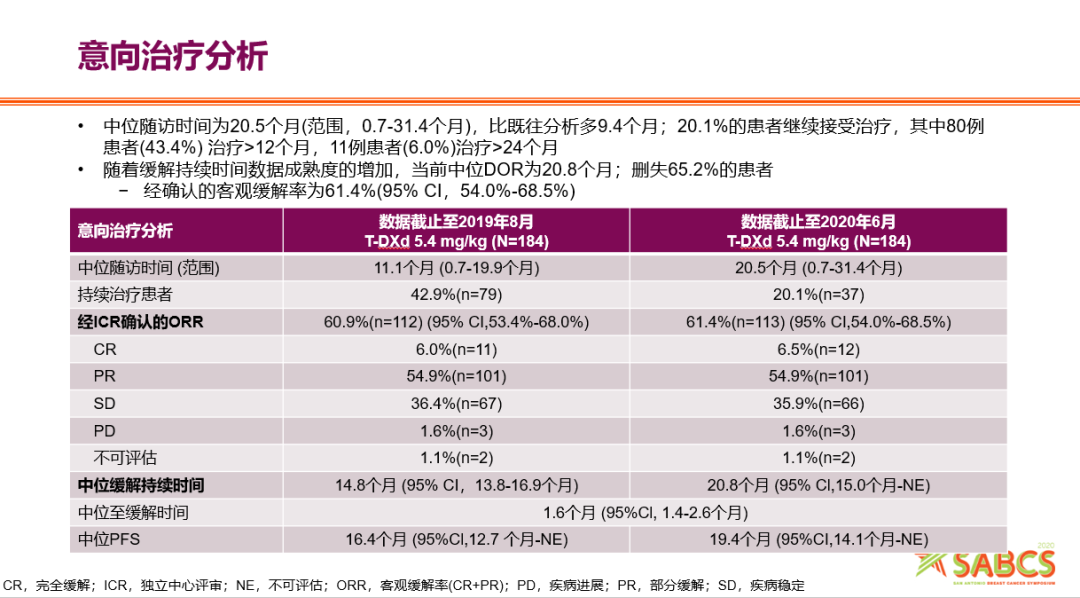
前言 DESTINY-Breast01研究是进一步探索T-DXd针对HER2阳性乳腺癌患者疗效和安全性的开放标签、多中心、两部分的II期研究。这两项研究成果多次亮相于圣安东尼奥乳腺癌会议(SABCS),并在美国临床肿瘤学会(ASCO)、欧洲肿瘤内科学会(ESMO)上同样大放光彩,丰硕的研究成果使之成为ADC药物里程碑式的临床研究。 DESTINY-Breast01(DB-01)首次报告:HER2阳性乳腺癌突破性进展 DB-01研究[5]是紧随A-J101研究开展的另一项针对HER2阳性乳腺癌患者应用T-DXd评估其疗效和安全性的II期研究。该研究同样包括了两个部分: 第一部分确定T-DXd的最佳推荐剂量(5.4 mg/kg、6.4 mg/kg、7.4 mg/kg); 第二部分确定该推荐剂量的有效性和安全性。主要研究终点为独立委员会评估的ORR。从2017年10月至2018年9月,共有253例患者在北美、亚洲和欧洲8个国家的72个中心接受了至少一剂T-DXd治疗,其中184例患者接受了推荐剂量(5.4 mg/kg)。 首次数据分析截止于2019年8月1日,在意向治疗分析中,患者的ORR高达60.9%(95%CI 53.4-68.0),中位随访时间为11.1个月(0.7-19.9),中位DOR为14.8个月(95% CI 13.8-16.9),中位PFS为16.4个月(95%CI 12.7-未达到),且不良反应可耐受。研究数据于2019年第42届SABCS会议初次公布,并同步发表于《新英格兰医学杂志》,一经披露,再度掀起了学术界对ADC药物应用于实体瘤高度关注的热潮。2019年10月,FDA授予了T-DXd优先审评资格[6],同年12月20日加速批准了T-DXd用于在转移性治疗中至少接受过两种抗HER2治疗的不可切除或转移性HER2阳性乳腺癌患者的治疗[7]。2020年3月25日,T-DXd也在日本获批用于既往接受过化疗且对标准治疗难治或不耐受的HER2阳性不可切除或复发性乳腺癌患者的治疗[8]。 图3. DB-01研究设计(RP2D:推荐的II期研究剂量) 专家点评:“前期惊艳结果,开启ADC药物应用于乳腺癌治疗的新希望” A-J101研究表明了T-DXd良好的耐受性和治疗活性,并呈现出了对疾病的持久控制。虽然该研究是一项I期临床研究,但其在多线治疗后HER2阳性乳腺癌患者以及HER2低表达乳腺癌患者中均显示出了优异的表现,开启了后续ADC药物治疗后线乳腺癌患者和HER2低表达患者靶向治疗的新希望。在剂量探索阶段也证实了5.4mg/kg剂量的安全性和有效性,为II期DB-01研究的成功奠定了坚实的基础。DB-01研究结果显示T-DXd不仅显著缓解了肿瘤进展,延长患者无进展生存时间,获得了惊艳结果,得到了FDA优先审评和快速上市的认定。与此同时,其他在研的乳腺癌ADC药物也随着这项研究结果出炉而备受关注。 三、DB-01研究更新:探索乳腺癌治疗的更多可能 2020年ASCO大会报道了基于15项临床特征对DB-01研究进行的多因素分析[9],结果表明所有亚组都具有显著的ORR获益和持续的疾病缓解,特别是当治疗线数仅为2线时,ORR高达76.7%,高于所有其他亚组,提示T-DXd更早线治疗获益。随后脑转移亚组分析数据在2020年ESMO Breast会议报告中公布,结果表明在24例基线伴有中枢神经系统(CNS)转移的亚组患者中,ORR达到58.3%(95% CI 36.6-77.9),中位PFS长达18.1个月(95% CI 6.7-18.1),这表明针对脑转移患者也具有潜在治疗获益。 A-J101研究和DB-01研究均验证了T-DXd针对HER2低表达乳腺癌患者,同样具有显著的抗肿瘤作用。2020 年ESMO大会公布的一项基于人工智能(Artificial Intelligence,AI)技术探索HER2表达水平和病理学特征用于预测T-DXd治疗获益人群的临床研究。该研究提取了A-J101研究中149例乳腺癌患者HER2切片和HE染色图像,结果显示,使用人工HER2评分筛选的HER2阳性和HER2阴性患者的ORR分别为53%和41% (p=0.29),而AI技术可测定完整的膜性HER2阳性乳腺癌细胞并增加细胞质HER2染色,比人工HER2评分筛选能识别出更多的T-DXd治疗获益患者(86% vs. 82%),ORR得到明显改善(55% vs. 24%,p <0.009)。因此,这种AI技术的应用有望为鉴别出更多在T-DXd获益的HER2低表达患者[10]。 2020年SABCS再次更新了DB-01研究,数据截止到2020年6月8日,中位随访时间为20.8个月,20.1%的患者仍在接受治疗,确认的ORR高达61.4%(包括12例CR),中位 DOR长达20.8个月,DCR高达97.3%,更新的中位PFS长达19.4个月,预估12个月的OS率高达85%((95% CI 79%-90%)),18个月的OS率高达74%(95% CI 67%-80%),预估的中位OS长达24.6个月(目前OS成熟度为35%),安全性数据与既往报道一致。再次有力验证了T-DXd在HER2阳性晚期乳腺癌领域的卓越疗效[11]。 图4. DB-01研究在2020年SABCS会议中的更新数据(意向治疗分析) 图5. DB-01研究在2020年SABCS会议中的更新数据(PFS&OS) 专家点评:成果斐然,引领HER2乳腺癌领域诊疗新模式 继DB-01研究首次公布于2019年SABCS会议,在2020年各大乳腺癌相关大会上也都可见T-DXd的“身影”,丰富的数据成果充分体现药物对于改善HER2阳性乳腺癌患者的生存获益具有重要价值。从它的亚组分析中可以看到,针对乳腺癌脑转移患者也显示出独特优势,为众多合并脑转移的乳腺癌患者从ADC药物中得到治疗获益创造了可能性。利用人工智能辅助诊断HER2表达的优化模式,也为筛选能从T-DXd治疗中获益的HER2低表达患者群体提供新的工具。作为ADC药物在晚期乳腺癌患者里程碑式的DB-01研究以及更早之前的A-J101研究打破了传统HER2治疗的模式,不仅在治疗效果上有了新的突破,同时也迈入了HER2低表达治疗领域,并将AI辅助的病理分子诊断与临床治疗更紧密地结合,引领ADC药物在HER2乳腺癌领域诊疗的新模式。 专家介绍 聂建云 教授 博士,主任医师,博士研究生导师 加拿大麦吉尔大学 博士后 云南省肿瘤医院乳腺三科 科主任 云南省高层次人才医学学科带头人 云南省有突出贡献优秀专业技术人才(“省突”)津贴获得者 中国抗癌协会 青年理事 中国CSCO乳腺癌专家委员会 常务委员 中国CSCO患者教育专家委员会 常务委员 中国抗癌协会乳腺癌专业委员会 委员 云南省医师协会乳腺癌专业委员会 主任委员 云南省抗癌协会乳腺癌专业委员会 副主任委员 主持国家自然科学基金课题3项,国际合作课题、省级部级课题及厅局级课题20余项。课题分别获云南省科技进步一等奖、三等奖、云南省卫生科技成果二等奖。在国内外刊物发表医学论文50余篇,SCI论文9篇。主编医学专著2部,参编医学专著7部。参与中国《CSCO乳腺癌诊疗指南》及相关共识的制定及编撰 [1] Doi T, Shitara K, Naito Y, et al. Safety, pharmacokinetics, and antitumour activity of tRAStuzumab deruxtecan (DS-8201), a HER2-targeting antibody-drug conjugate, in patients with advanced breast and gastric or gastro-oesophageal tumours: a phase 1 dose-escalation study. Lancet Oncol. 2017 Nov;18(11):1512-1522. [2]https://www.onclive.com/view/fda-grants-ds8201-breakthrough-designation-for-her2-breast-cancer [3] Modi S, Tsurutani JJ, Takahashi SJ, et al. Safety and efficacy results from a phase 1 study of DS-8201a in patients with HER2 expressing breast cancers.2017 SABCS. Abstract PD3-07. [4] Tamura K, Tsurutani J, Takahashi S, et al. TRAStuzumab deruxtecan (DS-8201a) in patients with advanced HER2-positive breast cancer previously treated with trastuzumab emtansine: a dose-expansion, phase 1 study. Lancet Oncol. 2019 Jun;20(6):816-826. [5] Modi S, Saura C, Yamashita T, et al. DESTINY-Breast01 Investigators. Trastuzumab Deruxtecan in Previously Treated HER2-Positive Breast Cancer. N Engl J Med. 2020 Feb 13;382(7):610-621. [7] https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-fam-trastuzumab-deruxtecan-nxki-unresectable-or-metastatic-her2-positive-breast-cancer [8]https://www.onclive.com/view/trastuzumab-deruxtecan-approved-in-japan-for-her2-metastatic-breast-cancer [9] Modi S, Andre F, Krop IE, et al. Trastuzumab deruxtecan for HER2-positive metastatic breast cancer: DESTINY-Breast01 subgroup analysis. J Clin Oncol 38: 2020 (suppl; abstr 1036). https://meetinglibrary.asco.org/record/185173/poster [10] Modi S, Glass B, Prakash A, et al. Artificial intelligence analysis of advanced breast cancer patients from a phase I trial of trastuzumab deruxtecan (T-DxD): HER2 and histopathology features as predictors of clinical benefit. 2020ESMO.Abstract 286P. https://www.annalsofoncology.org/article/S0923-7534(20)40384-9/fulltext [11] Modi S, Saura C, Yamashita T, et al. Updated results from DESTINY-Breast01, a phase 2 trial of trastuzumab deruxtecan (T-DXd ) in HER2 positive metastatic breast cancer. 2020 SABCS. PD3-06.